Хенрик Кессман, см. его публикации
«Последую примеру другого цитируемого здесь автора ЖЖ, — попробую пересказать эту статью вольным стилем на русском языке. Точный перевод названия статьи «Происхождение, эволюция и фенотипическое действие новых генов».
Авторы сосредоточены на выявлении всех известных на данный момент механизмов приобретения функционально полезных (адаптивных) новых генов, которые могут кодировать новый белок или новую некодирующую РНК (такие РНК обычно работают как регуляторы разнообразных внутриклеточных процессов). Важно отметить, что это не теоретическая разработка, а именно анализ реальных данных по геномам и по функциям генов.
1.Появление новых генов из дуплицированных предковых белок-кодирующих генов и генов некодирующих РНК
Содержание
- 1 1.Появление новых генов из дуплицированных предковых белок-кодирующих генов и генов некодирующих РНК
- 2 2. Откуда берутся промоторы для копий генов, образованных по механизму «обратная транскрипция—вставка в геном» (ретрогенов)
- 3 3. Функциональные следствия образования ретрогенов
- 4 4. К чему еще может привести ретротранспозиция
- 5 5. Включение кусков интронов в зрелую мРНК благодаря появлению новых или исчезновению старых сайтов сплайсинга
- 6 6. Образование новых генов путем слияния двух старых генов
- 7 7. Возникновение абсолютно новых генов из некодирующих и неповторяющихся областей генома
- 8 8. Участие одомашненных геномных паразитов в возникновении новых генов
- 9 9. Горизонтальный перенос генов
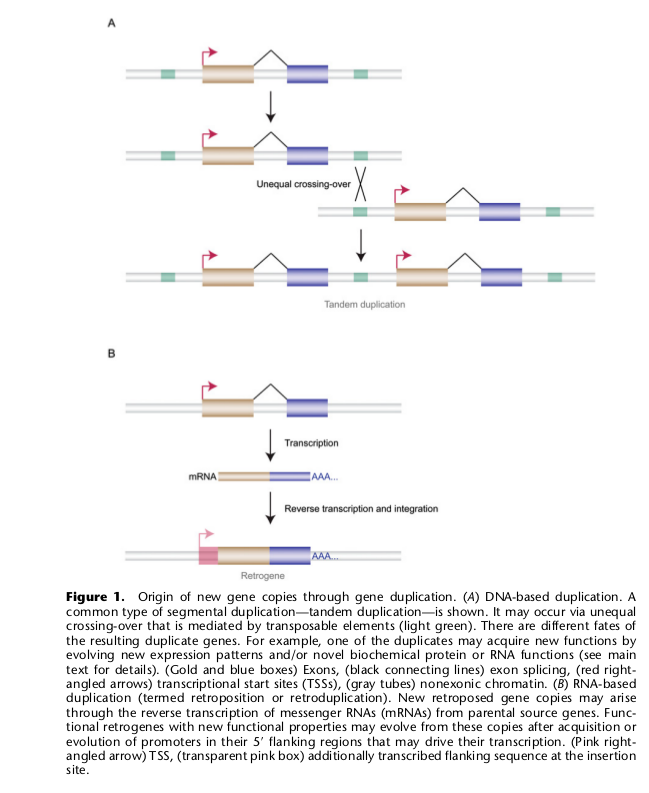
Для начала рассматривается хорошо известная схема, включающая:
1) дупликацию какого-то уже существующего гена, а затем 2) постепенное мутационное преобразование этого гена или обоих, которое может, при счастливом стечении обстоятельств, привести к появлению у этого гена (генов) новой функции. Дупликация может быть следствием а) неравного кроссинговера при мейозе (дупликация хромосомных сегментов); б) полиплоидизации генома (кратное увеличение полного набора хромосом; в) вставки в геном фрагментов ДНК, которые получились в результате обратной транскрипции с собственных РНК копий исходного гена (образование ретрокопий/ретрогенов).
Средняя частота дупликаций хромосомных сегментов у эукариот оценивается диапазоном 0,01-0,001 на ген в 1 миллион лет. Но в реальности такие события являются частыми для незначительного числа генов (1,6-3% генов) – и это все гены, отвечающие за формирование адаптаций к изменчивым условиям среды (например, гены иммунной системы); в то время, как для остальной части генов это крайне редкое событие. Интересно, что в линии человекообразных обезьян и гоминид такие дупликации встречаются чаще по сравнению с остальными приматами.
Частота образования ретрокопий генов намного ниже, чем дупликаций хромосомных сегментов. У млекопитающих, насекомых и растений встречается чаще, у птиц реже (и у них нет ретротранспозонов!). У человека в геноме есть тысячи ретрокопий, из них сотни — функциональные гены.
После появления двух копий гена возможны ситуации: а) когда старый ген сохраняет свою функцию, а новый приобретает новую функцию, либо б) когда оба гена, выполняющие исходно несколько функций сразу, разделяют обязанности между собой и специализируются в выполнении отдельных функций; в) когда оба гена сохраняют свою функцию, а из-за удвоения гена повышается количество синтезируемого продукта (РНК и белка); г) когда вторая копия оказывается нефункциональной и теряется со временем.
2. Откуда берутся промоторы для копий генов, образованных по механизму «обратная транскрипция—вставка в геном» (ретрогенов)
Обнаруживается целых 6 вариантов:
1) Ген может случайно вставиться рядом с GC-богатой областью, которая начинает работать как промотор.
2) Постепенное приобретение промоторной активности у близлежащей области благодаря накоплению точечных мутаций при поддержке положительного отбора.
3) Промоторную активность может проявлять область ретротранспозона, по которому произошла вставка гена в геном (потому что вставки как раз чаще всего в такие места с ретротранспозонами и происходят).
4) Транскрипция с альтернативных промоторов, содержащихся внутри копированного гена.
5) Вставка ретрогена внутрь кодирующей области какого-то другого гена вблизи точки начала транскрипции, и транскрипция с его промотора.
6) Если ген вставился где-то на расстоянии от промоторной области, то просто появляется либо дополнительный участок в 5’ нетранслируемой области, либо дополнительный полипептид на N-конце белкового продукта, если раньше начинается трансляция.3. Функциональные следствия образования ретрогенов
Оказывается, ретрогены значительно более склонны приобретать новую функцию, чем гены, дуплицированные в результате неравного кроссинговера. Оно и понятно: другой сегмент генома, следовательно, другое окружение, другие контуры регуляции, другие группы сцепления…Мало того, случается, что смысловой цепью в ретрогене становится нить , комплементарная той, что была смысловой в исходном гене, и тогда образуется совершенно новый белок, который выполняет совершенно новую функцию. Как это ни странно…
4. К чему еще может привести ретротранспозиция
При перемещении ретротранспозонов, типа L1, они могут прихватывать с собой область хромосомы, фланкирующую ретроэлемент с 3′ конца (из-за пропуска своего сайта терминации транскрипции). Если в этой области есть ген, то захватываются, соответственно, некоторые его части (допустим, область промотора с точкой начала транскрипции), и попадают в новые области генома, стимулируя возникновение новых генов в прежде не кодирующей области. В ряде случаев может перенестись и целый ген (если он небольшой).
5. Включение кусков интронов в зрелую мРНК благодаря появлению новых или исчезновению старых сайтов сплайсинга
Такой механизм не описан в этой статье, но описан в другой англоязычной статье последних лет. Новый сайт сплайсинга может появиться путем последовательных нуклеотидных замен, но гораздо легче — переноситься с все теми же транспозонами, в которых часто уже есть донорный и/или акцепторный сайт сплайсинга. Два таких элемента в разных частях интрона могут создать условия для включения части интрона в качестве экзона — авторы назвали такое явление «экзонизацией» («exonisation«).
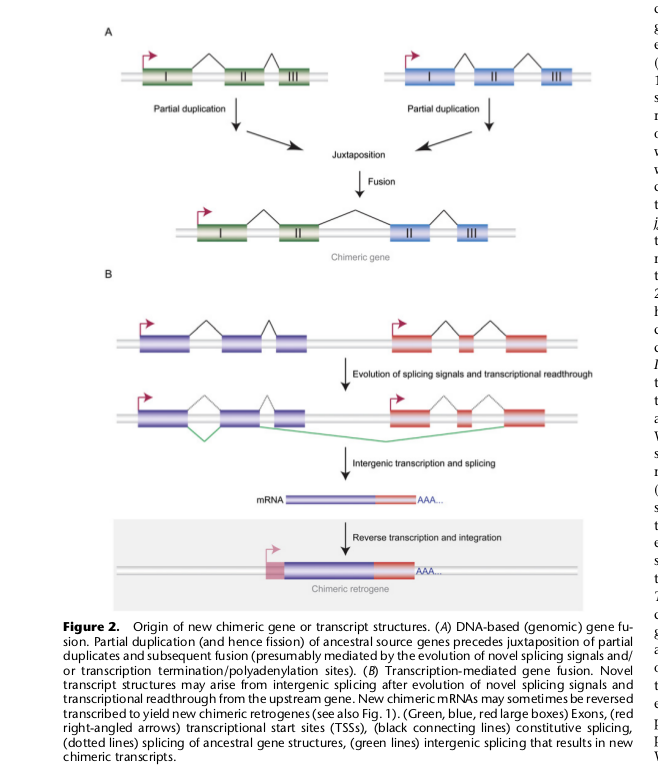
6. Образование новых генов путем слияния двух старых генов
В таком случае образуется ген, кодирующий белок, который может выполнять одновременно много функций — химерный белок с несколькими разными функциональными доменами. Есть три пути образования таких генов.
1) Первый -дупликация какого-то гена со встраиванием дуплицированной копии в рамку считывания другого гена, между его 5′ и 3′ концами.
2) Второй — возможен, если два исходных гена изначально расположены рядом на хромосоме и транскрибируются в одном направлении. Если произойдет утрата области терминации транскрипции в первом из них, то транскрипция будет идти до области терминации следующего, так что мРНК будет содержать последовательность сразу двух генов, а в результате сплайсинга этой мРНК и трансляции образуется химерный белок.
3) Про третий путь авторы статьи почему-то забыли — это рекомбинация между хромосомами в областях, находящихся внутри рамки считывания двух исходных генов. Вероятнее всего, это будет происходить в тех случаях, когда оба исходных гена содержат какие-то сходные участки, которые могут опять же появиться там вследствие ретродупликаций. Например, таким путем по-видимому образовался ген, кодирующий у нас бифункциональную аминоацил-тРНК синтетазу. Часть этого белка работает как глутамат-тРНК синтетаза, а часть — как пролин-тРНК синтетаза. У исходных разделенных генов есть сходный участок, который у одного гена находится с 3′, а у другого — с 5′ конца, и по этому участку и произошла транслокация, которая привела к их объединению.
7. Возникновение абсолютно новых генов из некодирующих и неповторяющихся областей генома
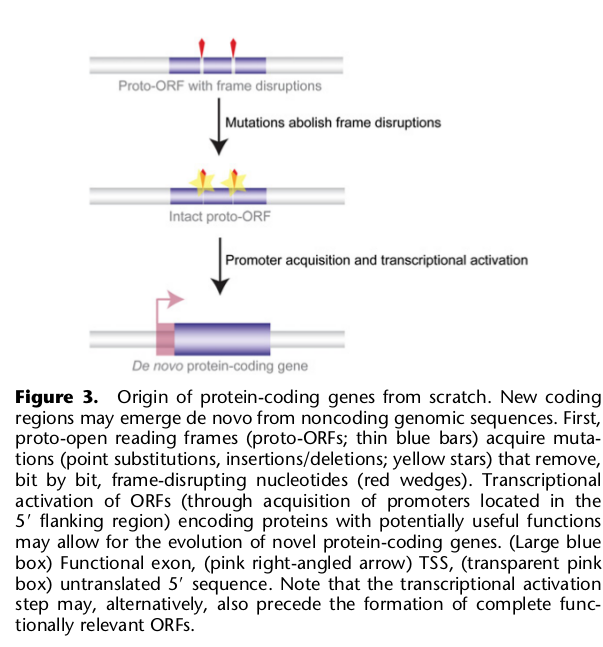
а) Белок-кодирующие гены
Здесь все определяется двумя условиями:
1) должна быть обеспечена возможность транскрипции, то есть должна появиться область промотора перед будущим геном. Как это может произойти — уже обсуждалось выше (пункт 2);
2) должны сформироваться элементы, которые обеспечат возможность трансляции с транскрибированной РНК. То есть сигналы инициации, терминации трансляции, сигнал полиаденилирования мРНК, сайты сплайсинга.
Здесь можно предположить возможность двух путей приобретения таких элементов: последовательные замены нуклеотидов, пока не получится работающий вариант либо опять же через заимствование от других генов путем дупликаций-встраиваний или как-то еще (как и с областью промотора). У приматов, и у человека, и у дрожжей, и у дрозофилл обнаружено достаточно большое число генов, которые даже частично не похожи ни на какие гены их ближайших предков, то есть генов, сформированных, вероятно, на основе прежде не кодирующей ДНК.
Самым интересным тут является вопрос о том, как происходило включение таких новых генов в генные сети. Вероятно, это должен быть достаточно длинный путь с постепенной подгонкой структуры гена путем последовательных точечных мутаций. Само собой, на начальном этапе зарождения жизни все первые гены должны были быть НОВЫМИ.
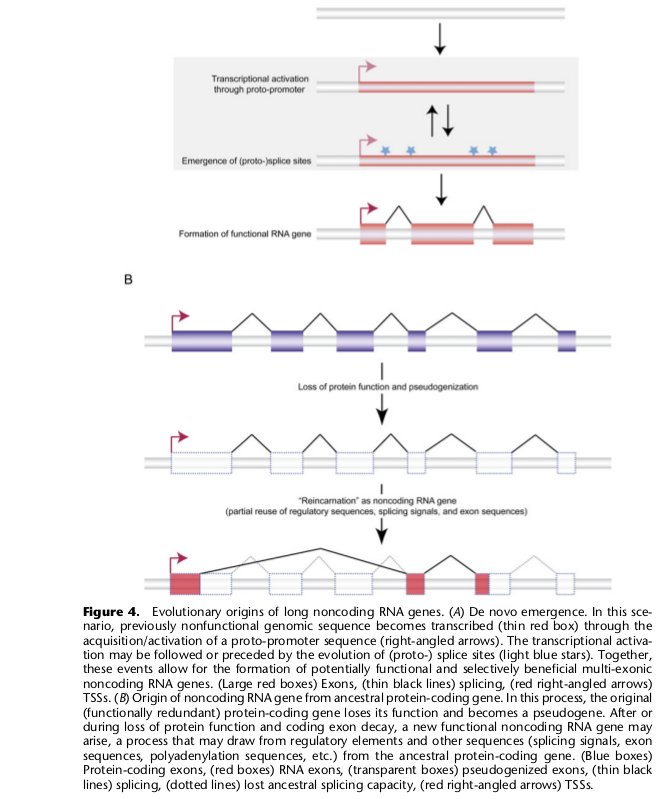
б) Гены некодирующих (регуляторных) РНК
Таких генов, скажем, в человеческом геноме насчитывают уже сотни для малых некодирующих и тысячи для длинных некодирующих РНК. Длинная не кодирующая РНК по-видимому может возникать в результате утраты некоторыми дуплицированными генами элементов, обеспечивающих их эффективную трансляцию. В частности, судя по всему, таким путем образовалась Xist РНК, участвующая в инактивации Х хромосомы. Сходным образом путем ретродупликаций могут возникать и гены малых не кодирующих РНК. В статье не говорится еще об одном варианте — когда некодирующая РНК образуется в результате активации транскрипции участка некодирующей (комплементарной) нити ДНК в области белок-кодирующего гена.
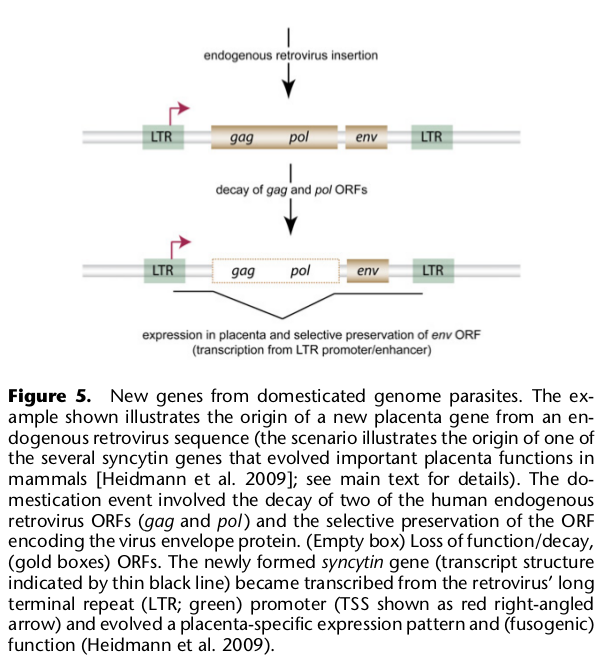
8. Участие одомашненных геномных паразитов в возникновении новых генов
Частично участие таких элементов — ретротранспозонов — уже было оговорено: они служат местами незаконных рекомбинаций, ведущих к дупликациям, они поставляют ферменты, участвующие в ретродупликациях и они сами могут приобретать функции регуляторных элементов (промоторов, энхансеров, сайленсеров и др.).
Но кроме того ретрогены могут включаться в качестве экзонов в белок кодирующие гены и выполнять функции, полезные для клетки. В частности, такое явление было показано для трех генов, участвующих в формировании плаценты, а также для одного из важных транскрипционных факторов, регулирующего экспрессию тысяч других генов клеткок млекопитающих. Из бывших ретротранспозонов также происходят некоторые гены не кодирующих длинных и малых регуляторных РНК.
9. Горизонтальный перенос генов
Существует несколько путей горизонтального переноса генов (горизонтальный перенос — это значит, что ген не унаследован от родителей, а получен как-то иначе от другого организма, причем организмы донора и реципиента могут быть одного вида или разных видов, даже очень отдаленных в эволюционном плане).
1) У прокариот существует механизм конъюгации, когда между двумя клетками-организмами образуется канал, по которому генетический материал может перетекать из одной клетки в другую. Может показаться, что для нас, эукариот, это не так уж важно, как там эти бактерии обмениваются генами. Но если вспомнить о том, что на определенном историческом этапе мы все прошли через микробную стадию, то станет понятно, что может быть этому обмену мы должны быть как раз прежде всего благодарны за то, чем мы стали теперь. Ведь гораздо проще эволюционировать, собирая в себе полезные гены, уже кем-то «изобретенные» в ходе эволюции, чем «изобретать» все разнообразие необходимых генов самостоятельно. Не зря прокариоты потратили на свою эволюцию 2 миллиарда лет, пока «изобрели» все, что необходимо. Весьма вероятно, что универсальный генетический код был выработан именно в процессе «коллективного творчества», связанного с активным взаимным горизонтальным обменом.
2) Мощными посредниками горизонтального переноса являются геномные паразиты типа ретровирусов, которые нечаянно могут прихватывать участки хромосом предыдущих хозяев и переносить к новым.
3) Горизонтальный перенос — нередкое событие в случае эндосимбиозов (от паразита к хозяину и обратно), например, от митохондрий и хлоропластов, — в прошлом бактерий-эндосимбионтов, в ядерный геном эукариот попало большое число генов самого разнообразного функционального назначения.
А еще много заимствованных генов от самых разных видов организмов, имеется у коловраток и инфузорий, хотя механизм переноса здесь остается неизвестным. Похоже на то, что они каким-то образом заимствуют гены от тех, кем питаются.
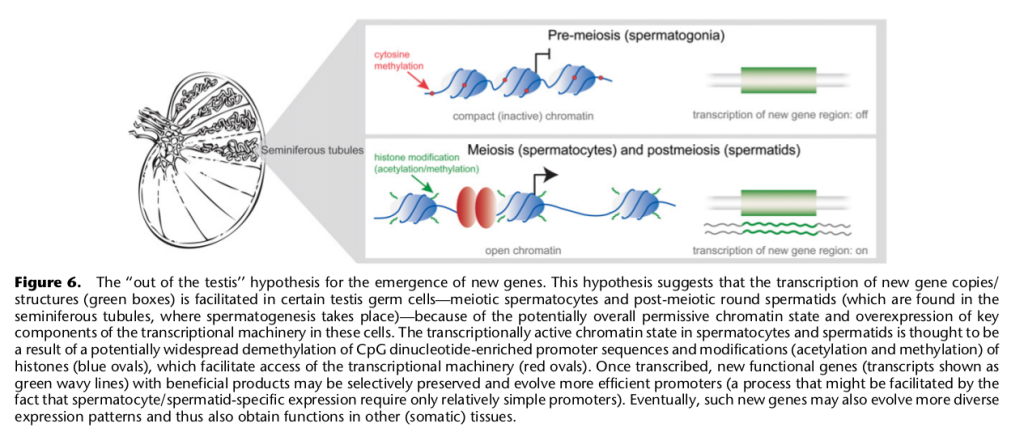
10. Сперматозоиды — как испытатели новых генов
Авторы делают любопытное замечание о том, что во-первых, в клетках предшественниках сперматозоидов новые гены возникают с довольно высокой частотой, и что во-вторых, на этапе мейоза и постмейоза этих клеток наблюдается активация экспрессии одновременно большого числа генов, включая и эти новые. Казалось бы, зачем сперматозоидам это надо? Об этом в статье ничего не написано, так что остается лишь строить предположения. Возможно это этап первичной проверки на наличие летальных мутаций? То есть очевидно, если возникла мутация, или новый ген, который полностью нарушает нормальное протекание внутриклеточного метаболизма, то такой сперматозоид должен будет погибнуть. А может быть тут подключается еще и иммунологическое тестирование новообразованных сперматозоидов на дефекты?
Источник biologist2
Оригинал в Genome Research
![О происхождении генов Print PDF «Последую примеру другого цитируемого здесь автора ЖЖ, — попробую пересказать эту статью вольным стилем на русском языке. Точный перевод названия статьи «Происхождение, эволюция и фенотипическое действие новых генов». […]](http://www.socialcompas.com/wp-content/uploads/2016/12/kaessmann-465x190.jpeg)